La dilution. Déterminer le volume final ou la concentration finale d'une solution aqueuse après une dilution (ex. : la concentration d'une solution diminue de moitié lorsque le volume du solvant est doublé). Tu as besoin d'aide? Pour plus d'informations sur ces concepts, tu peux consulter notre bibliothèque virtuelle pour des détails.. Le procédé par lequel le taux de concentration d'un corps solide ou liquide est diminué, par l'adjonction d'un produit solvant, se nomme la dilution. Le composé à diluer doit être soluble. Il est possible également d'obtenir une dilution en ôtant une partie de la solution initiale et de conserver son volume en ajoutant un solvant.

Document 4 1. Qu'estce qu'une dilution? 2. Lorsqu'on dilue un acide, comment évolue le pH ? 3

PDF facteur de dilution exercice PDF Télécharger Download
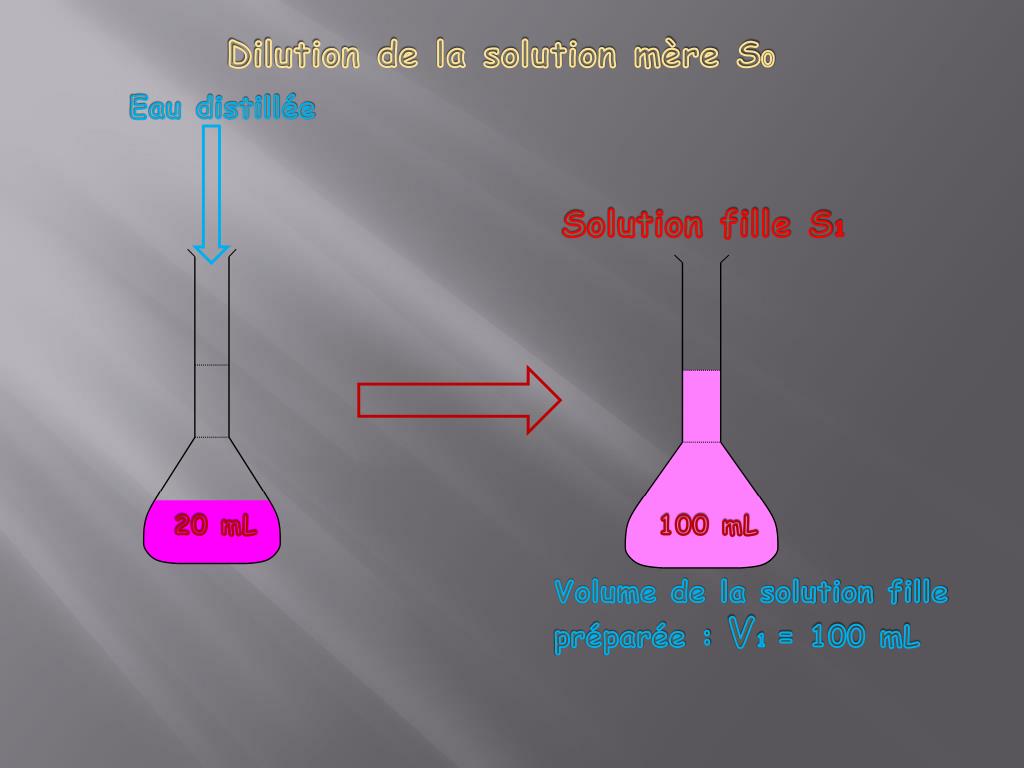
PPT Dilution d’une solution PowerPoint Presentation, free download ID2175289

Savoir réaliser la dilution d'une solution YouTube

DILUTION 🧪 Conservation de la Quantité de Matière Chimie Lycée YouTube

comment faire une dilution

La dilution pour les nuls des chimies argentiques

Dilution définition et explications AquaPortail

Exemple vidéo Dilution 2nde 4 YouTube

Différence Entre Dissolution Et Dilution Parlons Science

Les réactions aux solutions acides cours de 5eme SchoolMouv

A_Explication principe de dilution YouTube
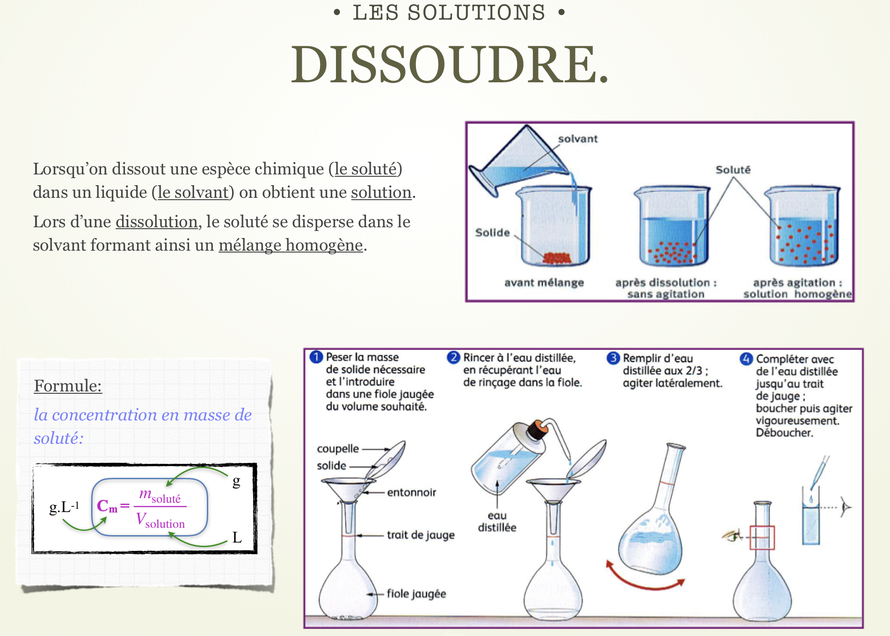
Les solutions Site de sciencesphysiquesolycee

Vidéo préparation d'une solution par dilution YouTube

La dilution d'une solution YouTube

Cours de Physiquechimie Concentration massique et dissolution Pipettes

⌚🧪 Qu'estce qu'une dilution ? ‖ Physiquechimie ‖ Collège YouTube
Dilution d'une solution cours to all

II Concentration massique et dilution YouTube

La dilution et la dissolution YouTube
Grâce à ses services d'accompagnement gratuits et stimulants, Alloprof engage les élèves et leurs parents dans la réussite éducative.. Le taux de dilution est le rapport du soluté (la substance à diluer) au solvant (par exemple, l'eau).Le liquide dilué doit être soigneusement mélangé pour obtenir une véritable dilution. Si vous avez une dilution de 1:3, c'est-à-dire un taux de dilution de 1:3, cela signifie que vous ajoutez 1 unité de volume de soluté (par exemple, de concentré) à 3 unités de volume du solvant.